|
СТРОЕНИЕ МОЛЕКУЛ. ХИМИЧЕСКАЯ СВЯЗЬ. ВАЛЕНТНОСТЬ ЭЛЕМЕНТОВ
Виды химической связи
Химическая связь — это взаимодействие двух атомов, осуществляемое путем обмена электронами. При образовании химической связи атомы стремятся приобрести устойчивую восьмиэлектронную (октет) или двухэлектронную (дублет) оболочки. Различают следующие виды химической связи: ковалентная (полярная и неполярная; обменная и донорно-акцепторная), ионная, водородная, металлическая.
Ковалентная связь. Связь, осуществляемая за счет образования электронной пары, принадлежащей обоим атомам, называется ковалентной. Различают обменный и донорно-акцепторный механизмы образования ковалентной связи.
1)Обменный механизм. Каждый атом дает по одному неспаренному электрону в общую электронную пару:
Н* +*Н > Н : H
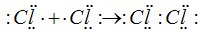
H:N:H L Н .
2)Донорно-акцепторный механизм. Один атом (донор) предоставляет электронную пару, а другой
атом (акцептор) предоставляет для этой пары свободную орбиталь:
Два атома могут обобществить несколько пар электронов. В этом случае говорят о кратных связях:
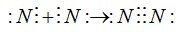
Если электронная плотность расположена симметрично между атомами, ковалентная связь называется неполярной. Если электронная плотность смещена в сторону одного из атомов, то ковалентная связь называется полярной. Полярность связи тем больше, чем больше разность электроотрицательностей атомов.
Электроотрицательность — это способность атома притягивать электронную плотность от других атомов. Самый электроотрицательный элемент — фтор, самый электроположительный — цезий.
Ионная связь. Если разность электроотрица-тельностей атомов велика, то электронная пара, осуществляющая связь, переходит к одному из атомов, и оба атома превращаются в ионы. Химическая связь между ионами, осуществляемая за счет электростатического притяжения, называется ионной связью.
Водородная связь — это связь между положи¬тельно заряженным атомом водорода одной молекулы и отрицательно заряженным атомом другой молекулы. Водородная связь имеет частично электро-статический, частично донорно-акцепторный характер.
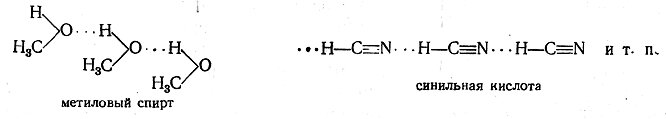
Водородная связь изображена точками.
Наличие водородной связи объясняет высокие температуры кипения воды, спиртов, карбоновых кислот.
Металлическая связь. Валентные электроны металлов достаточно слабо связаны со своими ядрами и могут легко отрываться от них. Поэтому металл содержит ряд положительных ионов, расположенных в определенных положениях кристаллической решетки, и большое количество электронов, свободно перемещающихся по всему кристаллу. Электроны в металле'осуществляют связь между ионами металла. Такой тип связи называется металлической связью.
Гибридизация орбиталей — это изменение формы некоторых орбиталей при образовании ковалентной связи для достижения более эффективного перекрывания орбиталей.
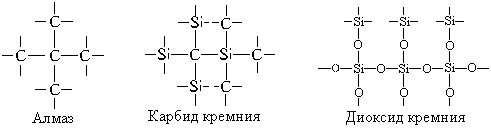
a) sp3Гибридизация. Одна s-орбиталь и три Молекулы, в которых осуществляется sp -гибридизация, имеют тетраэдрическую геометрию
(СН4, NHg).
б) sp2'Гибридизация. Одна s-орбиталь и две р-орбитали превращаются в три одинаковые орбитали, угол между осями которых равен 120
Гибридизация орбиталей Если связь образуется при перекрывании орбиталей по линии, соединяющей ядра атомов, она называется (5-связью. Если орбитали перекрываются вне линии, соединяющей ядра, то образуется К-связь.
Две sp-орбитали могут образовывать две ?-связи (ВеН2, ZnCl2). Еще две П-связи могут образоваться, если на двух р-орбиталях, не участвующих в гибри-дизации, находятся электроны. Пример — молеку-л а С2Н2.
р-орбитали превращаются в четыре одинаковые «гибридные» орбитали, угол между осями которых равен 109\28*
Три 5р2-орбитали могут образовывать три (7-связи (BF3, AlClg). Еще одна связь (7С-связь) может образоваться, если на р-орбитали, не участвующей в гибридизации, находится электрон. Пример — молекула С2Н4.
Молекулы, в которых осуществляется sp2-rn6-ридизация, имеют плоскую геометрию.
в) sp-Гибридизация. Одна орбиталь и одна р-орбиталь превращаются в две одинаковые орбитали, угол между осями которых равен 180'
Молекулы, в которых осуществляется sp-гибридизация, имеют линейную геометрию.
|
