|
Скорость химических реакций
 Скорость химической реакции определяется как скорость изменения молярной концентрации одного из реагирующих веществ. Скорость химической реакции определяется как скорость изменения молярной концентрации одного из реагирующих веществ.
Если при неизменных объеме и температуре концентрация одного из реагирующих веществ уменьшилась от C1 до с2 за промежуток времени от t1до t2, то скорость реакции за данный промежуток времени равна:
v = -(с2 - c1)/(t2 - t1) = -?с / ?t.
Химические реакции происходят при столкновении молекул, поэтому скорость реакции зависит от:
а)числа эффективных столкновений;
б)вероятности того, что столкновение приведет к превращению.
Число столкновений определяется концентрациями реагирующих веществ, а вероятность реакции — энергией сталкивающихся молекул (температурой).
Влияние концентрации. Зависимость скорости реакции от концентраций реагирующих веществ описывается основным законом химической кинетики — законом действующих масс:
Скорость химической реакции при постоянной температуре прямо пропорциональна произведению концентраций реагирующих веществ.
Для реакции
аА+ЬВ » сС + ...
скорость реакции в любой момент времени равна:
v = k(T)* [А]а * [В]ь,
где k(T) — константа скорости данной реакции, зависящая только от температуры. Физический смысл константы скорости заключается в том, что она равна скорости реакции при единичных концентрациях реагирующих веществ.
В зависимости от числа молекул, участвующих в столкновении, различают моно-, би- и тримолекулярные реакции:
1) Мономолекулярными называются реакции распада (или изомеризации):
А = С+ ...
Для мономолекулярных реакций закон действующих масс записывается в виде:
v = k(T) / [A]
2)Бимолекулярные — это реакции, которые происходят при столкновении двух молекул:
А+В=С+
V = k(T) • [А] • [В].
Пример. Н + Сl2 = НСl + Сl.
3)В тримолекулярных реакциях происходит одновременное столкновение трех молекул:
2А + В = С,
v — k * [А]2 • [В].
Пример: 2NO + 02 = 2N02.
Влияние температуры. Зависимость скорости реакции от температуры определяется константой скорости.
Правило Вант-Гоффа: при повышении температуры скорость большинства химических реакций возрастает в 2—4 раза при нагревании на каждые десять градусов.
Это правило связано с понятием температурного коэффициента скорости реакции ?:
? =v(T+ 10)/v(T) = 2 / 4. При увеличении температуры от T1 до Т2 изменение скорости можно рассчитать по формуле:
Правило Вант-Гоффа применимо только в узком интервале температур.
Более точным является уравнение Аррениуса, описывающее зависимость константы скорости от температуры:
k(T) = A * e-EA/(RT)
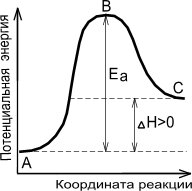
где А — постоянная, зависящая только от природы реагирующих веществ, R — универсальная газовая постоянная, ЕA— энергия активации, т. е. энергия, которой должны обладать сталкивающиеся молекулы, чтобы столкновение привело к химическому превращению. Для большинства реакций энергия активации составляет несколько десятков кДж/ моль.
Физический смысл энергии активации демонстрирует энергетическая диаграмма химической реакции
Чем больше энергия активации, тем сильнее возрастает скорость реакции при увеличении температуры.
Понятие о катализе. Катализатором называется вещество, увеличивающее скорость химической реакции, но остающееся неизменным после того, как химическая реакция заканчивается.
Механизм действия катализаторов связан с тем, что они уменьшают энергию активации за счет образования промежуточных соединений.
|
