|
Произведение растворимости.
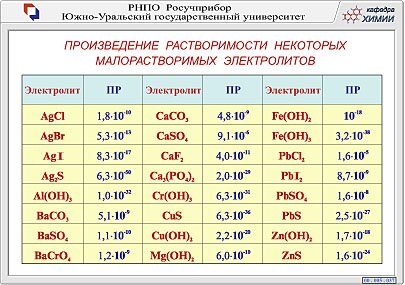
Диссоциацию малорастворимых веществ характеризуют с помощью специальной константы — произведения растворимости (ПР). Для электролита, диссоциирующего по уравнению
AB(тв) ? ? А++ В-
ПР(АВ) = [А+][В-]
Направление протекания ионных реакций. Реакции между ионами в растворах электролитов идут практически до конца в сторону образования: а) осадков, б) газов, в) слабых электролитов.
Примеры: а) Образование осадков.
BaCl2+ Na2SO4=BaSO4 ? +2NaCl
б) Образование газов:
CaCO3 + 2HCl = СаСl2 + С02? + Н20
или СаС03 + 2H+ = Са2+ + С02? + Н20.
NH4N03 + КОН = KNO3 + NH3? + H20
или NH4- + ОН- = NH3? + Н20.
в) Образование слабых электролитов (воды, слабых кислот и оснований, комплексных соединений).
НСl + NaOH = NaCl + H20, или
Н+ + ОН- = Н20.
2KF + H2S04 = K2S04 + 2HF, или
F- + Н+ = HF.
Во всех этих примерах реакции идут с образованием веществ с меньшей концентрацией ионов в растворе.
|
