|
Химическое равновесие
Химические реакции, которые при одних и тех же условиях могут идти в противоположных направлениях, называются обратимыми:
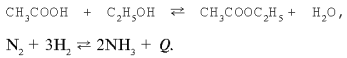
Реакцию, протекающую слева направо, называют прямой (константа скорости k1), справа налево —обратной (константа скорости k2)-
Состояние, в котором скорость обратной реакции становится равной скорости прямой реакции, называется химическим равновесием.
Состояние химического равновесия количественно характеризуется константой равновесия, которая представляет собой отношение констант скорости прямой и обратной реакции. Для обратимой реакции константа равновесия равна:
К = k1/k2 - ([С]p * [D]q)/([A]m [ВТ]n).
Данная формула выражает закон действующих масс для химического равновесия. В правую часть этой формулы входят равновесные концентрации участников реакции.
Константа равновесия зависит от температуры и природы реагирующих веществ.
Чем больше константа равновесия, тем больше равновесие смещено в сторону образования продуктов прямой реакции.
Смещение химического равновесия. Изменения, происходящие в равновесной системе в результате внешних воздействий, определяются принципом подвижного равновесия — принципом Ле Ша-телье:
Внешнее воздействие на систему, находящуюся в состоянии равновесия, приводит к смещению этого равновесия в направлении, при котором эффект произведенного воздействия ослабляется.
1) Если увеличить давление, то в равновесной системе будут развиваться реакции, происходящие с уменьшением давления, т. е. с уменьшением числа газообразных молекул.
2S02 + 02 ? ? 2S03,
2СН4 ? C2H2 + 3H2
Увеличение давления будет смещать равновесие первой реакции вправо, а второй реакции влево.
Если газовая реакция происходит без изменения числа молекул (N2 + 02 ? 2No), то давление не влияет на положение равновесия.
2) Если увеличить температуру, то в равновесной системе будут развиваться реакции, происходящие с уменьшением температуры, т. е. с поглощением теплоты (эндотермические реакции).
N2 + ЗН2 ? 2NH3 + 92,4 кДж,
N2 + 02 ? 2NO - 180,8 кДж.
Увеличение температуры будет смещать равновесие первой реакции влево, а второй реакции вправо
|
