|
Электронные конфигурации атомов
Теория Бора. Основные постулаты:
1. Электрон может вращаться вокруг ядра по строго определенным (стационарным) круговым орбитам. При движении по этим орбитам электрон не излучает энергию. Радиус орбиты г и скорость электрона v связаны квантовым соотношением. Бора:
mvr = nh/2П, где т — масса электрона, п — номер орбиты, h — постоянная Планка (h = 6,625 • 10~34 Дж • с).
2. Энергия излучается и поглощается только при переходе с одной орбиты на другую. Частота излучения (поглощения) V связана с энергией орбит соотношением:
Е1 -Е2 = hV.
Теория Бора справедлива только для атома водорода.
Квантовая теория строения атома. В основе современной теории строения атома (квантовой механики атома) лежат следующие основные положения:
1.Электрон имеет двойственную (корпускулярно-волновую) природу. Он может вести себя и как
частица, и как волна. Длина волны электрона X и его скорость v связаны соотношением де Бройля:
? = h/mv,
где т — масса электрона.
2.Для электрона невозможно одновременно точно измерить координату и скорость. Чем точнее мы измеряем скорость, тем больше неопределенность в координате, и наоборот. Математическим
выражением принципа неопределенности служит соотношение
?x * m * ? v > h/4П
где ? х — неопределенность положения координаты, ? v — погрешность измерения скорости.
3.Электрон в атоме не движется по определенным траекториям, а может находиться в любой части околоядерного пространства. Пространство вокруг ядра, в котором вероятность нахождения электрона достаточно велика, называют орбиталью.
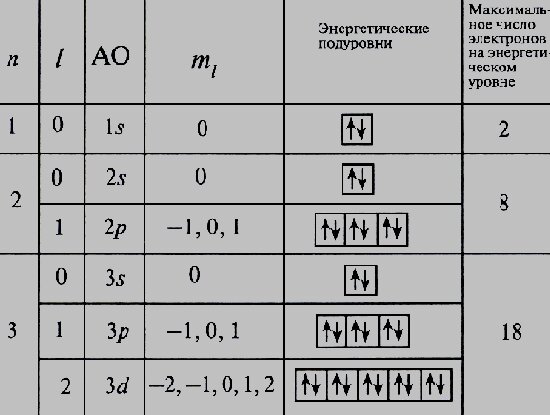
Квантовые числа электрона. Согласно квантовой механике, движение электрона в атоме описывается пятью квантовыми числами: главным n, побочным (орбитальным) l, магнитным ml, спиновым s и проекцией спина (магнитным спиновым числом) ms.
Главное квантовое число п определяет общую энергию электрона. Оно может принимать любые целые значения, начиная с единицы (n = 1, 2, 3, ...).
Побочное (орбитальное) квантовое число l характеризует форму орбитали. Оно может принимать целые значения от 0 до n - 1 (I = 0, 1, п - 1).
Обычно численные значения I принято обозначать следующими буквенными символами:
Значени 0 1 2 3 4
Буквенное обозначение sp d f g
В этом случае говорят о s-, р-, d-, f-, g- орбиталях.
Набор орбиталей с одинаковыми значениями л называется оболочкой (или энергетическим уровнем), с одинаковыми значениями n и l — подоболочкой (подуровнем), например: 2s-подуровень.
Магнитное квантовое число m характеризует направление орбитали в пространстве. Оно может принимать любые целые значения от —l до +1, включая 0, т. е. всего (2l + 1) значений. Например, при l = 1 ml = —1, 0, +1. При заданном главном
квантовом числе п возможна одна s-орбиталь, три р-орбитали, пять d-орбиталей и семь f-орбиталей.
Каждый электрон характеризуется спиновым квантовым числом s. Спин — это чисто квантовое свойство электрона, не имеющее классических аналогов. Для всех электронов абсолютное значение спина всегда равно s = 1/2. Проекция спина на ось z (магнитное спиновое число ms) может иметь лишь
два значения: тs= +1/2 или ms = -1/2.
Принципы заполнения орбиталей
1)Принцип Паули. В атоме не может быть двух
электронов, у которых все четыре квантовых числа
(n, l, ml и ms) были бы одинаковы.
Эквивалентное определение: на каждой орбитали может находиться не более двух электронов.
2)Принцип наименьшей энергии: в основном состоянии атома каждый электрон располагается так,
чтобы его энергия была минимальной.
Энергия орбиталей увеличивается в следующем порядке: Is < 2s < 2р < 3s < dp < 4s < < 3d < 4p < 5s < 4d < op < 6s < 4/ < 5d < 6p < < 7s < 5f < 6d < 7p.
Как видно из этого ряда, чем меньше сумма п + I, тем меньше энергия орбитали. При заданном значении п + I наименьшую энергию имеет орбиталь с наименьшим п.
3)Правило Гунда. В основном состоянии атом должен иметь максимально возможное число неспаренных электронов в пределах определенного подуровня.
Принцип наименьшей энергии и правило Гунда справедливы только для основных состояний атомов. В возбужденных состояниях электроны могут находиться на любых орбиталях атомов, если при этом не нарушается принцип Паули.
|
