|
Электролиты и электрическая диссоциация
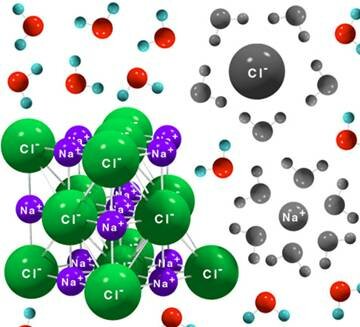
Все вещества принято условно делить по их поведению в растворах на две категории: а) вещества, растворы которых проводят ток (электролиты); б) вещества, растворы которых не проводят ток (неэлектролиты). К электролитам относится большинство неорганических кислот, оснований и солей. К неэлектролитам относятся многие органические соединения, например кетоны, углеводы. Распад электролитов на ионы при растворении в воде называется электролитической диссоциацией.
Основные положения теории электролитической диссоциации (С. Аррениус, 1887):
1. При растворении в воде электролиты распадаются на положительно и отрицательно заряженные ионы. Процесс диссоциации является обратимым.
2. Под действием электрического тока положительные ионы (катионы) движутся к катоду, отрицательные (анионы) — к аноду.
3. Степень диссоциации зависит от природы электролита и растворителя, концентрации электролита и температуры.
Степень диссоциации а — это отношение числа молекул, распавшихся на ионы (n , ), к общему числу растворенных молекул (n):
a=n , / n
Степень диссоциации а может изменяться от 0 (диссоциации нет) до 1 (полная диссоциация) и увеличивается с разбавлением раствора.
Электролиты со степенью диссоциации больше 30% обычно называют сильными, со степенью диссоциации от 3 до 30% — средними, менее 3% — слабыми электролитами.
К сильным электролитам относятся почти все соли, сильные кислоты (НС1, HBr, HI, HNO3, НС104,
H2S04(paзб)) и некоторые основания (LiOH, NaOH, КОН, Са(ОН)2> Sr(OH)2, Ba(OH)2). К слабым электролитам относятся слабые кислоты (H2S, H2SOg, СНдСООН, С6Н5ОН, H2Si03) и слабые основания.
Важной количественной характеристикой процесса диссоциации является константа диссоциации электролита. Для уравнения диссоциации электролита АК
АК? А- + К+
константа равновесия равна:
K=[ А- * К+]/ [AK]
Для электролитов типа АК константу диссоциации можно выразить через степень диссоциации а и молярную концентрацию С:
K=[ А- * К+]/ [AK]=a2/ 1-2 *C
|
