|
Анодные процессы
1) На инертном, или нерастворимом, аноде (графит, платина) возможны два процесса:
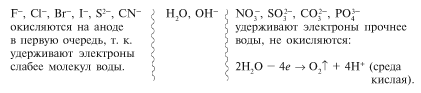
а) Если ионы кислотного остатка не содержат атомов кислорода, то окисляются именно они, например:
2Сl - - 2е----->Сl2
б) Если ионы кислотного остатка содержат атомы кислорода (SO|~ , NOg), то окисляются ионы ОН":
40 Н - - 4е------> 02 + 2Н20.
2) Если анод растворимый (медь, никель), то происходит окисление материала анода, и металл переходит в раствор в виде ионов, например:
Ni - 2e------>Ni2+
Количества веществ, выделившихся на электродах, определяют по уравнениям электродных реакций.Для этого находят кол-во электронов с помощью уравнения:
v(e) = I * t/F
Где I - сила тока(А),t - продолжительность электролиза(с);F = 96500 Кл/моль - константа Фарадея,равная заряду 1 моля электронов.
|
