|
ДАВЛЕНИЕ ГАЗА. ИДЕАЛЬНЫЙ ГАЗ
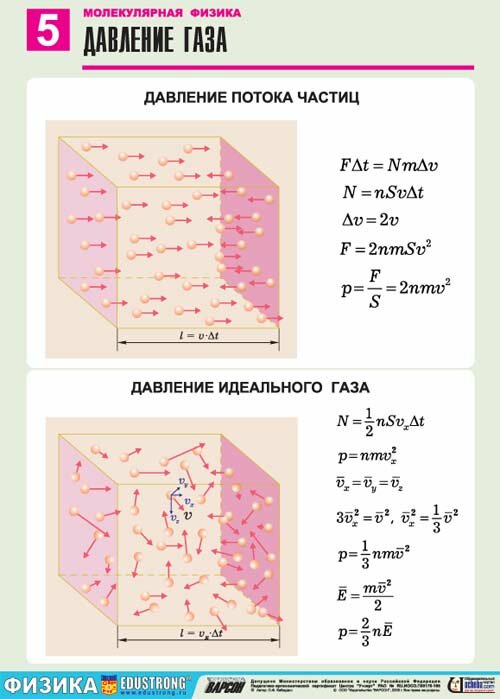
Давление, производимое газом на стенки сосуда, достаточно просто объясняется на основе МКТ газов. Это давление возникает вследствие того, что молекулы газа, беспорядочно двигаясь, ударяются о стенки сосуда, передавая им при каждом соударении свой импульс. Суммарный импульс, переданный за единицу времени единице площади, — это и есть давление, производимое газом.
Идеальный газ состоит из молекул, которые обладают пренебрежимо малым объемом по сравнению с объемом сосуда; между молекулами не действуют силы притяжения; при соударении молекул друг с другом и со стенками сосуда действуют силы отталкивания. Идеального газа в природе не существует — это упрощенная модель реального газа. Такое упрощение позволяет в ряде случаев гораздо легче решать практические задачи. Реальный газ становится близким по свойствам к идеальному, когда он достаточно нагрет и разрежен.
Существует два основных подхода к изучению газов: с учетом их молекулярного строения и использованием микропараметров (масса и скорость молекул, их концентрация и т. д.) и без учета молекулярного строения, когда газы описывают макропараметрами (давлением р, объемом V, температурой Т).
Между микро- и макропараметрами существует связь, которая выражается основным уравнением МКТ газов:
p=1/3m0nv2
Из этого уравнения видно, что давление газа увеличивается с ростом концентрации его молекул и скорости их движения.
Из основного уравнения МКТ газов также следует, что давление газа пропорционально произведению концентрации молекул на среднюю кинетическую энергию движения молекулы:
p=1/3m0nv2=2/3n * m0v2/2= 2/3nEK
Состояние газа описывается уравнением Менде леева—Клапейрона: pV'= m/M RT, где m — масса газа,
М — молярная масса газа, R = 8,31 ДжДмоль • К) — универсальная газовая постоянная.
Если масса газа m остается постоянной, то процесс изменения состояния газа можно описывать с помощью уравнения Клапейрона:
рV/T=const
Если при изменении состояния газа один из макропараметров (р, V или Т) остается постоянным (такие процессы принято называть изопроцессами), то из уравнения Клапейрона получаются частные газовые законы:
pV — const при Т = const — закон Бойля—Мариотта;
V/T= const при р =const — закон Гей-Люссака;
P/T=const при V —=const — закон Шарля.
|

Comments
RSS